아프다 세포, 시냅스 숫자와 인지 기능 유지에 악영향 줄 수 있어
세포의 성장과 분열 조절을 임의로 억제하는 방법 바꿔야

(내외방송=정지원 과학전문 기자) 노화된 뇌에서만 나타나는 새로운 세포가 발견돼 앞으로 노화를 극복하기 위해 세포 관련 분야의 활발한 연구가 진행될 전망이다.
KAIST는 8일 '내외방송'에 보낸 자료에서 "정원석 생명과학과 교수와 이은별 박사, 정연주 박사 연구팀이 노화된 뇌에서 기존에 알려지지 않은 새로운 종류의 별아교세포를 발견했다"며 "이 세포 내 단백질 항상성(안정적인 상태)이 손상돼 시냅스(신경 세포 간의 접합 부위) 생성과 제거 등의 능력이 결여돼 있다"고 밝혔다.
별아교세포는 뻗어 있는 많은 돌기가 마치 별처럼 보여 이름이 붙여졌으며 주로 뇌와 척수에 존재한다.
신경세포 사이를 메우는 역할을 해 영양 물질을 공급하거나 손상됐을 때 회복시키기도 한다.
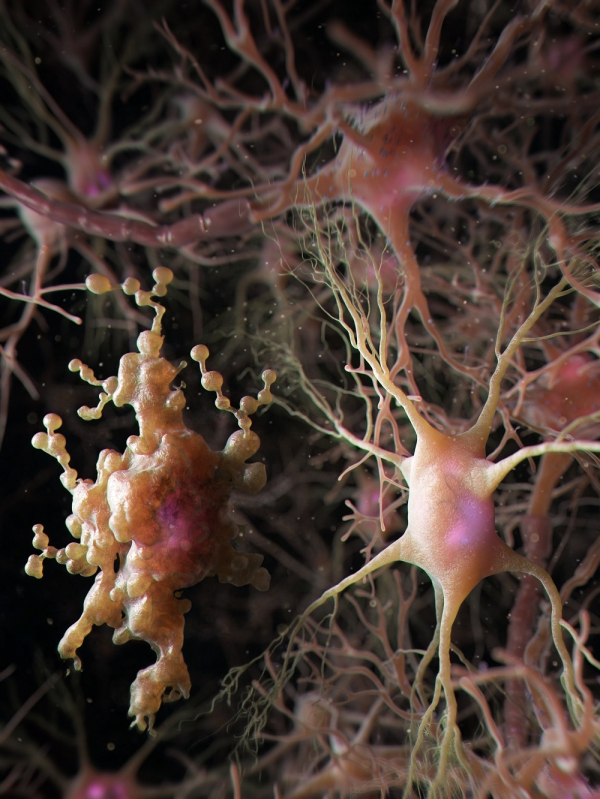
연구팀은 노화 및 치매가 진행되는 뇌에서 기억 중추인 해마(기억의 저장과 상기에 중요한 역할을 하는 기관)의 특이성으로 비정상적인 별아교세포가 생겨난다는 것을 최초로 관찰했다.
또, 시냅스의 숫자와 인지 기능 유지에 악영향을 준다는 것도 규명했다.
연구팀은 노화된 뇌에서 별아교세포의 기능 변화를 이해하고자 단일 세포 RNA의 시퀀싱(유전체 분석)을 수행했다.
그 결과 기존에 노화와 질병이 진행되는 뇌에서 존재한다고 알려진 염증성 별아교세포가 아니라 새로운 종류의 별아교세포인 '아프다(APDA: AutoPhagy-Dysregulated Astrocyte) 세포'가 존재한다는 것이 발견됐다.
새로운 별아교세포는 해마에서만 노화 과정에서 선택적으로 생기며 불필요한 단백질을 제거하는 자가포식 과정에서 만들어지는 오토파고솜(불필요한 단백질 등을 둘러싼 뒤 세포 내 작은 기관과 융합해 내용물을 소화하는 주머니 형태의 조직)이 축적돼 있다는 것도 알아냈다.
아프다 세포들에서는 다양한 단백질들이 원래 위치에서 벗어나 오토파고솜에 갇혀 있는 현상이 발견됐다.
이로 인해 별아교세포가 시냅스를 만들거나 제거하는 능력이 모두 상실된 것이다.
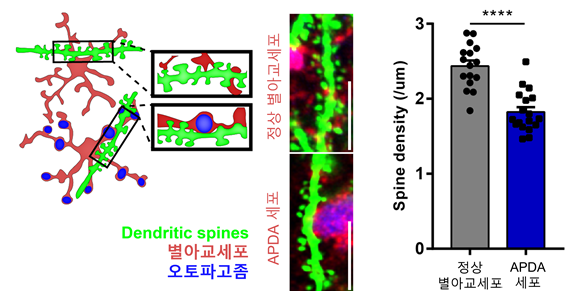
연구팀은 자가포식 작용이 비정상적으로 조절되고 있다는 것을 토대로 자가포식 작용에 영향을 주는 다양한 요소들을 연구했다.
그 결과 노화가 진행될수록 해마에 존재하는 별아교세포에서만 엠토르(세포의 성장과 분열을 조절)와 프로테아솜(단백질 분해 효소)의 활성도가 크게 감소한다는 것을 확인했다.
뿐만 아니라 원래 오토파고솜들은 리소좀에 의해 분해되는데, 아프다 세포들은 리소좀의 활성화도 감소해 있었다.
실제로, 연구진이 젊은 쥐에게 엠토르와 프로테아좀을 감소시키는 약물을 투입했더니 노화된 쥐에서 발견되는 아프다 세포를 만들 수 있었다.
이 쥐에서는 아프다 세포 주변 시냅스가 제대로 배열돼 있지 못하고, 숫자가 감소해 있어 인지 기능 저하를 일으킬 수 있다는 것을 보였다.
따라서 연구팀은 "현재 노화를 극복하기 위해 엠토르를 억제하려고 하는 방법이 오히려 아프다 세포의 생성을 촉진할 수 있다"고 강조했다.
한편, 이 연구는 삼성미래기술육성재단과 치매극복연구개발사업단의 도움을 받아 수행됐으며 국제학술지인 '네이처 에이징(Nature Aging)'에 지난 1일 온라인 공개됐다(논문명: A distinct astrocyte subtype in the aging mouse brain characterized by impaired portein homeostasis).