'역방향 알루 반복 구조', mRNA 기능 억제...암 발달 촉진
종양·노화 등 퇴행성 질환 치료 전략 마련하는 데 유용할 것

(내외방송=정지원 기자) 단백질 생산을 감소시키고, 다양한 질환 발병에서 핵심 역할을 하는 유전자 구조가 발견됐다.
6일 KAIST(한국과학기술원)에 따르면, 김유식 생명화학공학과 교수와 이영석 바이오및뇌공학과 교수 공동 연구팀이 종양 형성과 퇴행성 뇌질환을 유발하는 새로운 유전자 조절 원리를 밝혀냈다.
연구팀은 단백질 정보를 갖는 mRNA(DNA 유전정보를 세포질 속 소기관에 전달하는 역할) 유전자 조절 원리에서 '알루 요소'의 중요성을 제시했다. 알루 요소는 인간 유전체의 약 10%를 차지하는 반복서열로 mRNA의 단백질 생산 효율을 조절할 수 있는 것으로 알려졌다.
특히, mRNA가 알루 요소 2개로 구성된 '역방향 알루 반복 구조'를 갖게 되면 mRNA의 이동이 방해돼 단백질 생산이 감소한다. mRNA가 갖고 있는 유전자의 발현이 억제돼 질환을 일으키는 것이다.
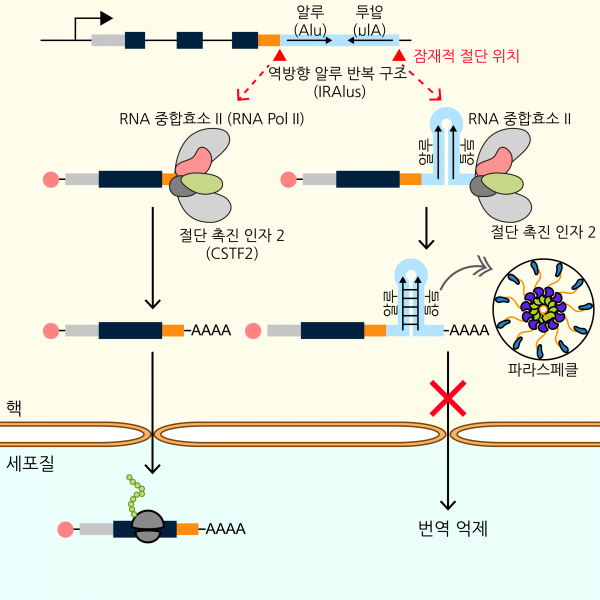
연구팀은 역방향 알루 반복 구조로 단백질 합성이 억제될 수 있는 mRNA 유전자 목록을 완성해 종양 형성 과정에서 영향력을 분석했다. 분석 결과, 종양억제유전자 활성을 억제한다고 알려진 특정 유전자가 활발해지면서 암 발달을 촉진한다는 것이 확인됐다.
뿐만 아니라 mRNA의 기능을 억제해 다양한 질병 치료와 조절 도구로 사용되고 있는 치료제 '올리고뉴클레오타이드'를 활용해 단백질 발현을 복구하는 암 치료 전략도 탐색했다.
이외에도 신경계 세포에서 역방향 알루 반복 구조로 유전자 조절이 과도하기 활성화되면 루게릭병(근육이 마비되는 질환) 등 퇴행성 뇌질환 간의 연관성을 최초로 제시했다.

김 교수는 "역방향 알루 반복 구조라는 새로운 물질을 활용하면 종양과 노화를 비롯한 다양한 퇴행성 질환의 발병 원리 분석에 효과적인 치료 전략을 마련하는 데 유용할 것"이라고 말했다.
구자영 생명화학공학과 박사와 이건용 박사과정이 공동 제1저자로 참여한 이번 연구는 한국연구재단 등의 지원을 받아 수행됐으며 국제학술지 '몰레큘러 셀(Molecular Cell)'에 최근 온라인 게재됐다(논문명: Alternative Polydenylation Determines the Functional Landscape of Inverted Alu Repeats).